N9E, infusionsvätska, emulsion
OLIMEL N9E
Infusionsvätska, emulsion Parenteral nutrition, kombinationer 4 x 1500 milliliter
Du behöver ett recept för att kunna köpa denna vara. Om du har ett recept kan du handla genom att logga in med ditt bank-ID.
Läs alltid bipacksedeln innan användning.
EAN: 07046260834095
Olimel
Läs noga igenom denna bipacksedel innan läkemedlet ges till dig. Den innehåller information som är viktig för dig.
Spara denna information, du kan behöva läsa den igen.
Om du har ytterligare frågor vänd dig till din läkare eller sjuksköterska.
Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt 4.
1. Vad Olimel N9E är och vad den används för
2. Vad du behöver veta innan du ges Olimel N9E
3. Hur Olimel N9E ges
4. Eventuella biverkningar
5. Hur Olimel N9E ska förvaras
6. Förpackningens innehåll och övriga upplysningar
1. Vad Olimel N9E är och vad den används för
Olimel N9E är en infusionsvätska, emulsion. Den tillhandahålls i en påse med tre sektioner.
En sektion innehåller en glukoslösning med kalcium, den andra innehåller en lipidemulsion och den tredje innehåller en aminosyralösning med elektrolyter.
Olimel N9E används för att ge näring till vuxna och barn över två års ålder genom en slang i en ven (infusion) när normalt näringsintag via munnen inte är lämpligt.
Olimel N9E får endast användas under medicinsk övervakning.
2. Vad du behöver veta innan du ges Olimel N9E
Använd inte Olimel N9E:
till för tidigt födda barn, nyfödda och barn yngre än 2 år.
om du är allergisk (överkänslig) mot ägg, sojabönsprotein, jordnötsprotein eller majs/majsprodukter (se också avsnitt “Varningar och försiktighet” nedan) eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6).
om du vet med dig att din kropp inte kan utnyttja vissa aminosyror
om du har särskilt höga fettnivåer i blodet.
om du har hyperglykemi (för mycket socker i blodet).
om du har en onormalt hög plasmakoncentration av någon elektrolyt (natrium, kalium, magnesium, kalcium och/eller fosfor).
I alla lägen kommer läkaren att grunda sitt beslut om du bör få detta läkemedel på faktorer som ålder, vikt och medicinska tillstånd, tillsammans med resultat från eventuella tester som utförts.
Varningar och försiktighet
Tala med läkare eller sjuksköterska innan Olimel N9E ges till dig.
Om du får nutritionslösningar via infusion (TPN) för snabbt kan det leda till skada eller dödsfall.
Infusionen måste avbrytas omedelbart om några onormala tecken eller symtom på allergisk reaktion (som svettning, feber, frossa, huvudvärk, hudutslag eller svårighet att andas) utvecklas. Den här produkten innehåller sojabönsolja och äggfosfolipider. Sojabönsprotein och äggprotein kan i sällsynta fall orsaka överkänslighetsreaktioner. Korsallergiska reaktioner mellan sojabönsprotein och jordnötsprotein har observerats.
Olimel N9E innehåller glukos som framställts av majs. Det kan orsaka överkänslighet (allergiska reaktioner) om du är allergisk mot majs eller majsprodukter (se avsnitt “Använd inte Olimel N9E” ovan).
Andningssvårigheter kan också vara ett tecken på att små partiklar har bildats som blockerar blodkärl i lungorna (utfällningar i lungkärlen). Om du uppleverandningssvårigheter, tala med läkareeller sjuksköterska. De kommer att fatta beslut om lämpliga åtgärder.
Ceftriaxon (ett antibiotikum) får inte blandas eller ges tillsammans med lösningar som innehåller kalcium (inklusive Olimel N9E) via dropp i en ven. Dessa läkemedel får inte ges tillsammans, inte ens om olika infusionsslangar eller infusionsställen används. Din läkare kan ge dig Olimel N9E och ceftriaxon efter varandra om infusionsslangar vid olika infusionsställen används eller om infusionsslangen byts ut eller spolas noggrant med fysiologisk koksaltlösning mellan infusionerna för att undvika utfällning (partiklar som bildats av ceftriaxon-kalciumsalt).
Vissa mediciner och sjukdomstillstånd kan öka risken för att utveckla en infektion eller sepsis (bakterier i blodet). Risken för infektion eller sepsis är särskilt stor när en slang (intravenös kateter) förs in i venen. Läkaren kommer att övervaka dig noggrant och vara uppmärksam på eventuella tecken på infektion. Patienter som behöver parenteral nutrition (näringstillförsel genom en slang i venen) kan löpa större risk för att utveckla infektion på grund av sitt sjukdomstillstånd. Risken för infektion kan minskas genom att man använder ”aseptisk teknik” (”bakteriefri teknik”) när man placerar och sköter om katetern och när man bereder näringslösningen (TPN).
Om du är allvarligt undernärd så att du behöver få näring genom en ven kommer din läkare att börja behandlingen långsamt. Din läkare kommer också att noggrant övervaka dig för att undvika plötsliga förändringar i vätske-, vitamin-, elektrolyt-, och mineralnivåerna.
Balansen mellan vatten och salt i kroppen och rubbningar i ämnesomsättningen kommer att rättas till före infusionen. Läkaren övervakar ditt tillstånd medan du får läkemedlet och kan ändra dosen eller ge dig ytterligare näringsämnen, t.ex. vitaminer, elektrolyter och spårämnen om han/hon finner det lämpligt.
Leversjukdomar, inkluderande problem med att göra sig av med gallan (kolestas), fettlever, fibros (bindvävsbildning), som kan leda till leversvikt, liksom gallblåseinflammation och gallsten i gallblåsan, har rapporterats hos patienter som får intravenös näring. Orsaken till dessa sjukdomar anses bero på flera faktorer och kan variera mellan olika patienter. Om du får symtom som illamående, kräkningar, buksmärtor, gulfärgning av hud eller ögon, kontakta din läkare för att identifiera möjliga orsaker och bidragande faktorer och möjliga behandlingar och förebyggande åtgärder.
Läkaren ska känna till följande tillstånd:
allvarliga problem med njurarna. Informera även din läkare om du får dialys eller annan typ av rening av blodet
allvarliga leverproblem
problem med blodkoagulationen
binjurar som inte fungerar som de ska (binjuresvikt). Binjurarna är triangelformade körtlar som sitter ovanpå njurarna.
hjärtsvikt
lungsjukdom
vattenansamling i kroppen (hyperhydrering)
otillräcklig mängd vatten i kroppen (dehydrering)
högt blodsocker (diabetes mellitus) som inte behandlas
hjärtattack eller chock på grund av plötslig hjärtsvikt
allvarlig metabolisk acidos (när blodet är för surt)
generaliserad infektion (septikemi)
koma.
För att kontrollera effekten och kontinuerligt övervaka att infusionen sker säkert utför läkaren kliniska tester och laboratorietester medan du får detta läkemedel. Om du får detta läkemedel i flera veckor övervakas din blodstatus regelbundet.
Om din kropp har nedsatt förmåga att göra sig av med fetterna i detta läkemedel kan ”fettöverbelastningssyndrom” uppkomma (se avsnitt 4 - Eventuella biverkningar).
Om infusionsstället ömmar, bränns eller svullnar under infusionen, eller om infusionen läcker, ska du berätta det för läkaren eller sjuksköterskan. Infusionen avbryts omedelbart och påbörjas i en annan ven.
Om ditt blodsocker blir för högt ska läkaren justera hastigheten för infusionen av Olimel N9E eller ge dig läkemedel som kontrollerar blodsockret (insulin).
Olimel N9E kan endast ges via en slang (kateter) i en stor ven i bröstet (centralven).
Barn och ungdomar
Om ditt barn är under 18 år kommer särskild försiktighet vidtas för att ge rätt dos. Fler säkerhetsåtgärder kommer också att vidtas, eftersom barn har en högre känslighet för infektioner. Tillsatser av vitaminer och spårämne krävs alltid. Läkemedelsformer som är anpassade till barn ska användas.
Andra läkemedel och Olimel N9E
Tala om för läkare om du tar eller använder eller nyligen har tagit eller använt eller kan tänkas ta eller använda andra läkemedel.
I normala fall är det inga problem att använda andra läkemedel samtidigt med detta läkemedel. Tala om för läkare om du tar eller nyligen har tagit några andra läkemedel, även receptfria sådana för att kontrollera att de går bra att ta samtidigt.
Tala om för din läkare om du använder eller får något av följande läkemedel:
Insulin
Heparin.
Olimel N9E får inte ges samtidigt som blod genom samma slang.
Olimel N9E innehåller kalcium. Det får inte ges tillsammans med eller genom samma slang som ceftriaxon (ett antibiotikum) eftersom partiklar då kan bildas. Om samma slang används för att ge dig dessa läkemedel efter varandra ska den sköljas noggrant.
Olimel N9E får inte ges i samma infusionslinje eller blandas tillsammans med ampicillin (antibiotikum) eller fosfenytoin (antiepileptika) på grund av risken för utfällning.
Oliv- och sojabönsoljan i Olimel N9E innehåller K-vitamin. Detta påverkar normalt inte blodförtunnande läkemedel (antikoagulantia) såsom kumarin, men du ska tala om för läkaren om du tar blodförtunnande läkemedel
Fetterna i denna blandning kan påverka resultaten av vissa laboratorietester om blodprov tas innan fetterna har försvunnit från ditt blodomlopp (vanligtvis har de försvunnit 5 till 6 timmar efter att infusionen avslutats).
Olimel N9E innehåller kalium. Särskild försiktighet bör iakttas för patienter som tar diuretika, ACE -hämmare eller angiotensin II-receptorantagonister (läkemedel mot högt blodtryck) eller immunsuppressiva läkemedel. Dessa typer av läkemedel kan öka kaliumnivåerna i blodet.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du får detta läkemedel.
Det saknas tillräckliga data från användningen av Olimel N9E hos gravida kvinnor och kvinnor som ammar. Vid behov kan Olimel N9E övervägas som behandling under graviditet och amning. Olimel N9E ska endast ges till gravida och ammande kvinnor efter noggrant övervägande.
Körförmåga och användning av maskiner
Ej relevant.
3. Hur Olimel N9E ges
Dosering
Olimel N9E ska endast ges till vuxna och barn över två år.
Olimel N9E är en infusionsvätska, emulsion som ges via en slang (kateter) in i en ven i bröstet.
Olimel N9E ska anta rumstemperatur före användning.
Olimel N9E är endast för engångsbruk.
Att ge en påse via infusion tar vanligtvis mellan 12 och 24 timmar.
Dosering – vuxna
Läkaren anger en flödeshastighet som motsvarar dina behov och ditt kliniska tillstånd.
Behandlingen kan fortsätta så länge som det behövs, beroende på ditt kliniska tillstånd.
Dosering – barn över 2 års ålder och ungdomar
Läkaren avgör vilken dos och under hur lång tid läkemedlet ska ges. Det beror på ålder, vikt, längd, medicinskt tillstånd och kroppens förmåga att bryta ner och tillgodogöra sig innehållsämnena i Olimel N9E.
Om du har fått för stor mängd av Olimel N9E
Om dosen är för hög eller infusionen sker för snabbt kan aminosyrorna göra blodet för surt, och tecken på hypervolemi (ökning av cirkulerande blodvolym) kan uppkomma. Glukosnivåerna i blodet och urinen kan öka, hyperosmolärt syndrom (för hög viskositet i blodet) kan utvecklas och fettinnehållet kan öka triglyceridmängden i blodet. En alltför snabb infusion eller stor volym av Olimel N9E kan framkalla illamående, kräkningar, frossa, huvudvärk, värmevallningar, överdriven svettning (hyperhidros) och störningar i elektrolytbalansen. Om något av detta inträffar måste infusionen avbrytas omedelbart.
I vissa allvarliga fall kan läkaren behöva ge tillfällig njurdialys för att hjälpa njurarna att göra sig av med överskottsprodukten.
För att förhindra detta kommer läkaren övervaka ditt tillstånd och testa dina blodvärden regelbundet.
Rådfråga läkare vid ytterligare frågor om hur man använder denna produkt.
4. Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem. Om du märker någon förändring i hur du mår under eller efter behandlingen, kontakta omedelbart läkare eller sjuksköterska.
Testerna som läkaren utför medan du tar detta läkemedel ska minimera risken för biverkningar.
Om några onormala tecken eller symtom på allergisk reaktion utvecklas, t.ex. svettning, feber, frossa, huvudvärk, hudutslag eller andningssvårigheter, ska infusionen avbrytas omedelbart.
Följande biverkningar har rapporterats för Olimel N9E:
Vanliga: kan förekomma hos upp till 1 av 10 användare:
Hjärtklappning (takykardi)
Nedsatt aptit
Ökad koncentration av fett i blodet (hypertriglyceridemi)
Buksmärtor
Diarré
Illamående
Förhöjt blodtryck (hypertoni).
Har rapporterats: förekommer hos okänt antal användare
Överkänslighetsreaktioner inklusive svettning, feber, frossa, huvudvärk, hudutslag (hudrodnad (erytematös), knottrig hud (papulös), varblåsor i huden (pustulös), fläckig hud (makulär), generaliserat utslag), klåda, värmevallningar, andningssvårigheter
Infusionsläckage till omgivande vävnad (extravasation) som kan ge smärta, irritation, svullnad/ödem, rodnad (erytem)/hetta, d�öda vävnadsceller (hudnekros) eller blåsor/vesiklar, inflammation, förtjockad eller stramande hud.
Kräkningar.
Följande biverkningar har rapporterats för liknande läkemedel för parenteral nutrition:
Mycket sällsynta: kan förekomma hos upp till 1 av 10 000 användare:
Försämrad förmåga att göra sig av med fetter (fettöverbelastningssyndrom) som är förenat med en plötslig och abrupt försämring av patientens medicinska tillstånd. Följande tecken på fettöverbelastningssyndrom försvinner oftast när infusionen av lipidemulsionen stoppas:
Feber
Minskat antal röda blodkroppar som kan leda till blek hud, svaghet och andfåddhet (anemi)
Lågt antal vita blodkroppar, vilket kan öka infektionsrisken (leukopeni)
Lågt antal blodplättar, vilket kan öka risken för blåmärken och/eller blödningar (trombocytopeni)
Koaguleringssjukdomar som påverkar blodets koagulationsförmåga
Höga fettnivåer i blodet (hyperlipidemi)
Inlagring av fett i levern (hepatomegali)
Försämrad leverfunktion
Symtom i centrala nervsystemet (t.ex. koma).
Har rapporterats: förekommer hos okänt antal användare:
Allergiska reaktioner
Onormala blodtester för kontroll av leverns funktion
Problem med att göra sig av med gallan (kolestas)
Förstorad lever (hepatomegali)
Leversjukdom i samband med parenteral nutrition (näringstillförsel genom en slang i venen) (se avsnitt 2 “Varningar och försiktighet”)
Ikterus (gulsot)
Minskat antal blodplättar (trombocytopeni)
Ökade kvävenivåer i blodet (azotemi)
Förhöjda leverenzymer
Bildande av små partiklar som kan blockera blodkärl i lungorna (utfällningar i lungkärlen) och orsaka lungemboli och andningssvårigheter.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera eventuella biverkningar direkt till Läkemedelsverket, www.lakemedelsverket.se. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Läkemedelsverket
Box 26
751 03 Uppsala
5. Hur Olimel N9E ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd detta läkemedel före utgångsdatum som anges på behållaren och den yttre förpackningen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Får ej frysas.
Förvaras i ytterpåsen.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
6. Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
De aktiva substanserna i varje påse av färdigberedd emulsion är 14,2 % (motsvarar 14,2 g/100 ml) L-aminosyralösning (alanin, arginin, glycin, histidin, isoleucin, leucin, lysin (som lysinacetat), metionin, fenylalanin, prolin, serin, treonin, tryptofan, tyrosin, valin, asparaginsyra, glutaminsyra) med elektrolyter (natrium, kalium, magnesium, fosfat, acetat, klorid), 20 % (motsvarar 20 g/100 ml) lipidemulsion (raffinerad olivolja och raffinerad sojaolja) och 27,5 % (motsvarar 27,5 g/100 ml) glukoslösning (som glukosmonohydrat) med kalcium.
Övriga innehållsämnen är:
Sektion med lipidemulsion | Sektion med aminosyralösning | Sektion med glukoslösning |
|---|---|---|
Renade äggfosfolipider, glycerol, natriumoleat, natriumhydroxid (för pH-justering), vatten för injektionsvätskor | Koncentrerad ättiksyra (för pH-justering), vatten för injektionsvätskor | Saltsyra (för pH-justering), vatten för injektionsvätskor |
Läkemedlets utseende och förpackningsstorlekar
Olimel N9E är en infusionsvätska, emulsion förpackad i en påse med tre sektioner. En sektion innehåller en fettemulsion, den andra en aminosyralösning med elektrolyter och den tredje en glukoslösning med kalcium. Sektionerna separeras av icke-permanenta förseglingar. Före administrering ska innehållet i sektionerna blandas genom att rulla ihop påsen med början från den övre änden tills förseglingarna är öppna.
Utseende före blandning
aminosyra- och glukoslösningarna är klara, färglösa eller lätt gulfärgade.
fettemulsionen är homogen och mjölkaktig.
Utseende efter blandning: homogen mjölkaktig blandning
Påsen med tre sektioner är tillverkad i flerskiktad plast. Påsmaterialets inre skikt (kontaktskiktet) är utformat så att det är kompatibelt med innehållsämnena och de godkända tillsatserna.
För att undvika kontakt med syre från luften är påsen förpackad i en ytterpåse som syrebarriär. Den innehåller en liten påse med en syreabsorberare .
Förpackningsstorlekar
1000 ml påse: 1 kartong med 6 påsar
1500 ml påse: 1 kartong med 4 påsar
2000 ml påse: 1 kartong med 4 påsar
1 påse à 1000 ml, 1500 ml och 2000 ml
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Baxter Medical AB
Box 63
164 94 Kista
Tillverkare
Baxter S.A.
Boulevard René Branquart, 80
7860 Lessines
Belgien
Denna bipacksedel ändrades senast: 2020-06-15
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal
Farmakoterapeutisk grupp: Lösningar för parenteral nutrition/blandningar
ATC-kod: B05 BA10.
A. KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Olimel N9E tillhandahålls i en påse med 3 sektioner.
Varje påse innehåller en glukoslösning med kalcium, en lipidemulsion och en aminosyralösning med elektrolyter.
Innehåll per påse | |||
1000 ml | 1500 ml | 2000 ml | |
27,5 % glukoslösning (motsvarar 27,5 g/100 ml) | 400 ml | 600 ml | 800 ml |
14,2 % aminosyralösning (motsvarar 14,2 g/100 ml) | 400 ml | 600 ml | 800 ml |
20 % lipidemulsion (motsvarar 20 g/100 ml) | 200 ml | 300 ml | 400 ml |
Sammansättning hos den färdigberedda emulsionen efter att de tre sektionerna blandats:
a Blandning av raffinerad olivolja (cirka 80 %) och raffinerad sojaolja (cirka 20 %) motsvarande en kvot essentiella fettsyror/fettsyror totalt på 20 %.
Övriga hjälpämnen är:
Sektion med lipidemulsion | Sektion med aminosyralösning och elektrolyter | Sektion med glukoslösning |
|---|---|---|
Renade äggfosfolipider, glycerol, natriumoleat, natriumhydroxid (för pH-justering), vatten för injektionsvätskor | Koncentrerad ättiksyra (för pH-justering), vatten för injektionsvätskor | Saltsyra (för pH-justering), vatten för injektionsvätskor |
Näringsintag för färdigberedd emulsion per p�åsstorlek:
1000 ml | 1500 ml | 2000 ml | |
|---|---|---|---|
Lipider | 40 g | 60 g | 80 g |
Aminosyror | 56,9 g | 85,4 g | 113,9 g |
Kväve | 9,0 g | 13,5 g | 18,0 g |
Glukos | 110,0 g | 165,0 g | 220,0 g |
Energi: | |||
Kalorier totalt (cirka) | 1070 kcal | 1600 kcal | 2140 kcal |
Icke-proteinkalorier | 840 kcal | 1260 kcal | 1680 kcal |
Glukoskalorier | 440 kcal | 660 kcal | 880 kcal |
Lipidkaloriera | 400 kcal | 600 kcal | 800 kcal |
Icke-proteinkalorier/kväve-kvot | 93 kcal/g | 93 kcal/g | 93 kcal/g |
Glukos-/lipidkalorier-kvot | 52/48 | 52/48 | 52/48 |
Lipidkalorier/kalorier totalt | 37 % | 37 % | 37 % |
Elektrolyter: | |||
Natrium | 35,0 mmol | 52,5 mmol | 70,0 mmol |
Kalium | 30,0 mmol | 45,0 mmol | 60,0 mmol |
Magnesium | 4,0 mmol | 6,0 mmol | 8,0 mmol |
Kalcium | 3,5 mmol | 5,3 mmol | 7,0 mmol |
Fosfatb | 15,0 mmol | 22,5 mmol | 30,0 mmol |
Acetat | 54 mmol | 80 mmol | 107 mmol |
Klorid | 45 mmol | 68 mmol | 90 mmol |
pH-värde | 6,4 | 6,4 | 6,4 |
Osmolaritet | 1310 mOsm/l | 1310 mOsm/l | 1310 mOsm/l |
a Inkl. kalorier från renade äggfosfolipider.
b Inkl. fosfat som kommer från lipidemulsionen.
B. DOSERING OCH ADMINISTRERINGSSÄTT
Dosering
Olimel N9E rekommenderas inte till barn under 2 år beroende på olämplig sammansättning och volym (se avsnitt 4.4, 5.1 och 5.2 i produktresumén).
Den maximala dagliga dosen som nämns nedan bör ej överskridas. På grund av flerkammarpåsens fasta komposition, kan patientens totala nutritionsbehov inte alltid tillgodoses. Vid vissa kliniska situationer kan patienten behöva en dos näringsämnen som inte täcks av påsens fasta sammansättning. I en sådan situation måste volym (dos)- justeringens effekt på doseringen av alla övriga näringsämnen i Olimel N9E beaktas.
Till vuxna
Doseringen beror på patientens energiförbrukning, kliniska status, kroppsvikt och förmåga att metabolisera innehållsämnena i Olimel N9E, liksom på extra energi- eller proteintillskott som ges oralt/enteralt. Därför skall påsstorleken väljas i enlighet med detta.
De genomsnittliga dagliga behoven är:
0,16 till 0,35 g kväve/kg kroppsvikt (1 till 2 g aminosyror/kg), beroende på patientens nutritionsstatus och graden av katabolism
20 till 40 kcal/kg
20 till 40 ml vätska/kg eller 1 till 1,5 ml per förbrukad kcal.
För Olimel N9E bestäms den maximala dagliga dosen av vätskeintaget, 35 ml/kg, motsvarande 2 g/kg aminosyror, 3,9 g/kg glukos, 1,4 g/kg lipider, 1,2 mmol/kg natrium och 1,1 mmol/kg kalium. För en patient som väger 70 kg skulle detta motsvara 2 450 ml Olimel N9E per dag, vilket resulterar i ett intag på 140 g aminosyror, 270 g glukos och 98 g lipider (dvs. 2 058 icke-proteinkalorier och 2 622 kalorier totalt).
I normala fall behöver flödeshastigheten ökas gradvis under den första timmen och sedan anpassas med hänsyn till dosen, den dagliga tillförda volymen och infusionens varaktighet.
För Olimel N9E är den maximala infusionshastigheten 1,8 ml/kg/timme, motsvarande 0,10 g/kg/timme aminosyror, 0,19 g/kg/timme glukos och 0,07 g/kg/timme lipider.
Till barn över 2 års ålder och ungdomar
Inga studier har genomförts för den pediatriska populationen.
Doseringen beror på patientens energiförbrukning, kliniska status och kroppsvikt och förmåga att metabolisera innehållsämnena i Olimel N9E, liksom extra energi- eller proteintillskott som ges oralt/enteralt. Därför skall påsstorleken väljas i enlighet med detta.
Dessutom minskar dagsbehovet av vätska, kväve och energi med åldern. Två åldersgrupper beaktas, 2 till 11 år och 12 till 18 år.
För Olimel N9E är den begränsande faktorn i åldersgruppen 2 till 11 år magnesiumkoncentrationen med avseende på daglig dos, och glukoskoncentrationen med avseende på infusionshastigheten. I gruppen 12 till 18 år är aminosyra- och magnesiumkoncentrationen den begränsande faktorn med avseende på daglig dos och aminosyrakoncentrationen med avseende på infusionshastighet. Det resulterar i följande intag:
2 till 11 år | 12 till 18 år | |||
Beståndsdel | Rekommendationa | Olimel N9E max. volym | Rekommendationa | Olimel N9E max. volym |
Maximala dagliga doser | ||||
Vätska (ml/kg/dag) | 60 - 120 | 25 | 50 - 80 | 35 |
Aminosyror (g/kg/dag) | 1 - 2 (upp till 2,5) | 1,4 | 1 - 2 | 2,0 |
Glukos (g/kg/dag) | 1,4 - 8,6 | 2,8 | 0,7 - 5,8 | 3,9 |
Lipider (g/kg/dag) | 0,5 - 3 | 1,0 | 0,5 - 2 (upp till 3) | 1,4 |
Energi totalt (kcal/kg/dag) | 30- 75 | 26,8 | 20 - 55 | 37,5 |
Maximal infusionshastighet per timme | ||||
Olimel N9E (ml/kg/timme) | 3,3 | 2,1 | ||
Aminosyror (g/kg/timme) | 0,2 | 0,19 | 0,12 | 0,12 |
Glukos (g/kg/timme) | 0,36 | 0,36 | 0,24 | 0,23 |
Lipider (g/kg/timme) | 0,13 | 0,13 | 0,13 | 0,08 |
a Rekommenderade värden från ESPGHAN/ESPEN/ESPR Guidelines, 2018
I normala fall behöver flödeshastigheten ökas gradvis under den första timmen och sedan anpassas med hänsyn till dosen, den dagliga tillförda volymen och infusionens varaktighet.
I allmänhet rekommenderas att infusionen för små barn startar på en låg daglig dos och att den ökas gradvis upp till den maximala dosen (se ovan).
Administreringssätt och behandlingslängd
Endast för engångsbruk.
Det rekommenderas att innehållet används omedelbart efter att påsen har öppnats och får inte sparas för en senare infusion.
Utseende efter rekonstitution: homogen vätska med ett mjölkaktigt utseende.
För anvisningar om beredning och hantering av denna infusionsvätska, emulsion, se avsnitt 6.6 i produktresumén.
På grund av dess höga osmolaritet kan Olimel N9E endast administreras via en central ven.
Den rekommenderade infusionstiden för en parenteral nutritionspåse är mellan 12 och 24 timmar.
Behandling med parenteral nutrition kan fortsätta så länge som patientens kliniska tillstånd kräver det.
C. INKOMPATIBILITETER
Tillsätt inte andra läkemedel eller substanser till någon av påsarnas sektioner eller till den färdigberedda emulsionen utan att först bekräfta deras kompatibilitet och stabiliteten hos den slutliga beredningen (särskilt lipidemulsionens stabilitet).
Inkompatibiliteter kan till exempel uppstå vid alltför hög surhetsgrad (lågt pH) eller olämpligt innehåll av tvåvärda katjoner (Ca2+ och Mg2+) vilket kan destabilisera lipidemulsionen.
Som med alla parenterala näringsblandningar måste kalcium- och fosfatkvoten beaktas. För stor tillsats av kalcium och fosfat, speciellt i form av mineralsalter, kan leda till att kalciumfosfatutfällningar bildas.
Olimel N9E innehåller kalciumjoner medför ökad risk för utfälld koagulering i citrat-antikoagulerat blod eller blodkomponenter.
Ceftriaxon får inte blandas eller administreras tillsammans med intravenösa lösningar som innehåller kalcium, inklusive Olimel N9E, genom samma infusionsslang (t.ex. via Y-koppling) på grund av risken för utfällning av ceftriaxon-kalciumsalt (se avsnitt 4.4 och 4.5 i produktresumén). Lösningar som innehåller ceftriaxon och kalcium får administreras sekventiellt efter varandra om infusionsslangar vid olika infusionsställen används, eller om infusionsslangen byts ut eller spolas ordentligt med fysiologisk koksaltlösning mellan infusionerna för att undvika utfällning.
Olimel N9E ska inte administreras i samma infusionslinje eller blandas tillsammans med ampicillin eller fosfenytoin på grund av risken för utfällning.
Kontrollera kompatibiliteten med lösningar som administreras samtidigt genom samma aggregat, kateter eller kanyl.
Olimel N9E får inte administreras före, samtidigt som eller efter blod genom samma utrustning på grund av risken för pseudoagglutination.
D. SÄRSKILDA ANVISNINGAR FÖR DESTRUKTION OCH ÖVRIG HANTERING
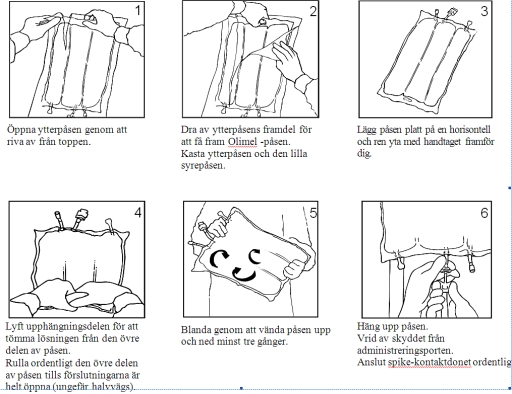
En översikt över de förberedande stegen för administrering av Olimel N9E ges i figur 1.
Öppna
Avlägsna den skyddande ytterpåsen.
Kasta den lilla påsen med syreabsorberaren.
Kontrollera att påsen och de icke-permanenta förslutningarna är oskadda. Använd endast om påsen är oskadad och de icke-permanenta förslutningarna är intakta (dvs. de tre sektionernas innehåll har inte blandats), om aminosyralösningen och glukoslösningen är klara, färglösa eller lätt gulfärgade, praktiskt taget fria från synliga partiklar och om lipidemulsionen är en homogen vätska med mjölkliknande utseende.
Blanda lösningarna och emulsionen
Kontrollera att produkten har antagit rumstemperatur när de icke-permanenta förslutningarna bryts.
Rulla för hand ihop påsen med början från påsens övre ände (änden med upphängningen). De icke-permanenta förslutningarna öppnas från den sidan som är närmast portarna. Fortsätt att rulla påsen tills förslutningarna är öppna längs halva sin längd.
Blanda genom att vända påsen upp och ned minst tre gånger.
Blandningens utseende efter beredning är en homogen mjölkliknande emulsion.
Tillsatser
Påsen är tillräckligt stor för att tillsatser som vitaminer, elektrolyter och spårämnen skall kunna tillsättas.
Alla tillsatser (inklusive vitaminer) kan göras i den färdigberedda blandningen (efter att de icke-permanenta förslutningarna har öppnats och innehållet i de tre sektionerna har blandats).
Vitaminer kan också tillsättas i glukossektionen innan blandningen har beretts (innan de icke-permanenta förslutningarna har öppnats och innan de tre sektionerna har blandats).
När tillsatser görs till beredningar som innehåller elektrolyter ska den mängd elektrolyter som redan finns i påsen tas med i beräkningen.
Tillsatser måste göras under aseptiska förhållanden och av kvalificerad personal.
Elektrolyter kan tillsättas i Olimel N9E enligt tabellen nedan:
Per 1000 ml | |||
Inkluderad nivå | Maximal ytterligare tillsats | Maximal total nivå | |
Natrium | 35 mmol | 115 mmol | 150 mmol |
Kalium | 30 mmol | 120 mmol | 150 mmol |
Magnesium | 4,0 mmol | 1,6 mmol | 5,6 mmol |
Kalcium | 3,5 mmol | 1,5 (0,0a) mmol | 5,0 (3,5a) mmol |
Oorganisk fosfat | 0 mmol | 3,0 mmol | 3,0 mmol |
Organisk fosfat | 15 mmolb | 10 mmol | 25 mmol b |
a Värdet motsvaras av tillsatsen av oorganisk fosfat.
b Inkluderar fosfat som kommer från lipidemulsionen.
Spårämnen och vitaminer:
Stabilitet har demonstrerats för vitamin- och spårämnespreparat som finns i handeln (innehållande upp till 1 mg järn).
Information om kompatibilitet för andra tillsatser finns på begäran.
Att göra en tillsats:
Iaktta aseptiska förhållanden.
Förbered påsens injektionsport.
Punktera injektionsporten och injicera tillsatserna med en injektionsnål eller
en beredningsanordning.
Blanda innehållet i påsen och tillsatserna.
Förbereda infusionen
Iaktta aseptiska förhållanden.
Häng upp påsen.
Avlägsna plastskyddet från adminstreringsporten.
För in infusionsaggregatets spike ordentligt i administreringsporten.
Figur 1. Beredningssteg för administrering av Olimel N9E
Administrering
Endast för engångsbruk
Administrera produkten först efter att de icke-permanenta förslutningarna mellan de tre sektionerna har brutits och innehållet i de tre sektionerna har blandats.
Kontrollera att den slutliga emulsionen för infusion inte visar några tecken på fasseparation.
Efter att påsen öppnats måste innehållet användas genast. Den öppnade påsen får aldrig sparas för en senare infusion. Återanslut aldrig en delvis förbrukad påse.
Seriekoppla inte påsarna, risk finns att gasemboli kan uppstå på grund av gasrester i den primära påsen.
Ej använt läkemedel, avfall och alla berörda instrument ska kasseras.
Extravasation
Övervaka kateterområdet regelbundet för att identifiera tecken på extravasation.
Om extravasation förekommer ska administreringen avbrytas omedelbart. Katetern eller kanylen ska sitta kvar så att patienten kan få omedelbar hjälp. Om möjligt ska vätskan aspireras genom den insatta katetern/kanylen så att mängden vätska minskar i vävnaderna innan katetern/kanylen tas bort.
För alla skador som orsakats av den extravaserade produkten (inklusive den produkt/de produkter som blandas med Olimel N9E om tillämpligt) ska specifika åtgärder vidtas i enlighet med skadans skede/omfattning. Behandlingsalternativen kan omfatta icke-farmakologiska, farmakologiska och/eller kirurgiska ingrepp. Om extravasationen är stor ska en plastikkirurg rådfrågas inom de närmaste 72 timmarna.
Extravasationsområdet ska övervakas minst var fjärde timme under de första 24 timmarna, därefter en gång per dag .
Infusionen får inte påbörjas på nytt i samma centrala ven.